PI3K/Akt/mTOR信号通路是哺乳动物肿瘤免疫中重要的信号通路,与细胞生长、增殖、转录、翻译、自噬、凋亡以及血管新生等密切相关。该通路的激活与肿瘤的发生紧密相关,可以增加肿瘤细胞的耐药性,抑制肿瘤细胞的凋亡,导致肿瘤进展。
该通路的上游成员PI3Ks(磷脂酰肌醇3-激酶,phosphoinositide 3-kinase)是高度保守的脂质激酶家族,根据结构特点和底物分子可将其分为Ⅰ型、Ⅱ型、Ⅲ型三类。PI3K是由一个催化亚基p110和一个调节亚基p85构成的异二聚体,ⅠA型PI3K与肿瘤关系最为密切,其根据催化亚基p110的不同又可分为PI3Kα、PI3Kβ 和PI3Kδ等3个亚型。编码PI3Kα的基因PIK3CA是肿瘤中最常见的突变。PIK3CA突变后在异常激活PI3Kα的同时,还能抑制抑癌基因PTEN的表达,因此PI3Kα历来都是各种肿瘤的抗癌药物研发中极为重要的靶点。PIK3CA在乳腺癌中的突变率高达40%,且主要集中在Luminal型和HER2基因扩增型乳腺癌,其中管腔A型中占45%,管腔B型中占30%。邵志敏教授团队对基于复旦队列的中国人群乳腺癌中PI3K/AKT信号通路基因的测序,结果与TCGA和COSMIC数据库类似:PIK3CA突变频率高达44%。
基础与临床研究均提示该基因突变与通路异常激活可促进非激素依赖的转录功能,造成内分泌治疗耐药;同时诸多证据也提示抗HER2靶向治疗和化疗的耐药与其也有着千丝万缕的关系。值得一提的是与ESR1突变不同,PIK3CA在乳腺癌转移灶与原发灶的突变率基本一致,提示在肿瘤早期即可能出现该基因的突变。
所谓小分子大能量,诸多证据证实该通路靶点的异常状态预示着更多的耐药与更差的预后,应予更积极的关注与治疗,但初期的相关探索却因为副作用与毒性严重限制了进展。
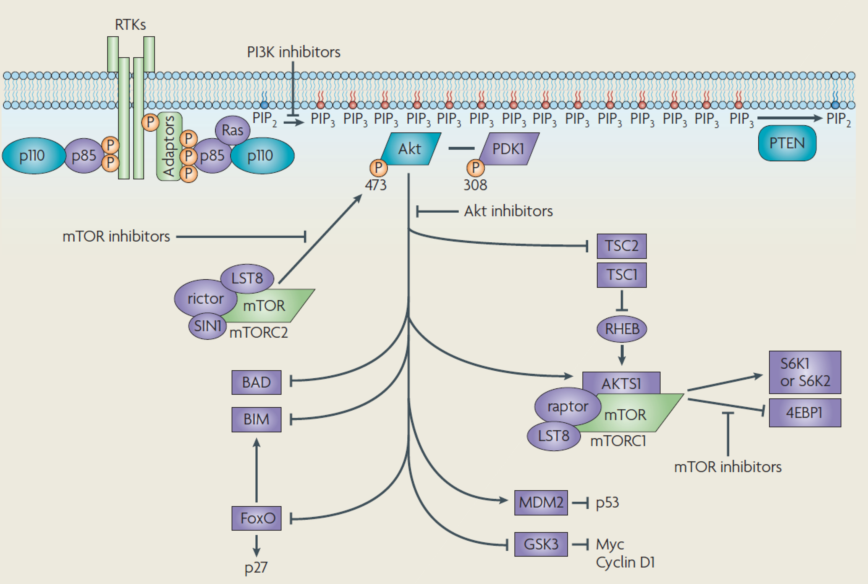
图1. ⅠA型PI3K信号通路
初期方向着力于逆转PI3Kα这一内分泌耐药的靶点,但既往研究均因为缺乏特异性的抑制、差强人意的疗效和不可控的毒副作用而铩羽而归。
BELLE-2研究的数据显示:泛PI3K抑制剂buparlisib对于携带PIK3CA突变的内分泌治疗耐药的晚期乳腺癌患者具有一定的疗效,却因为毒性大、耐受性差而限制了使用;SANDPIPER研究也在评估Taselisib(PI3Kα和PI3Kβ的选择性抑制剂)疗效时,因为2个月PFS的“温柔获益”而转身去寻找更高特异性抑制PI3Kα和更好安全性的药物。究其原因:PI3K各亚型之间的ATP结合位点几乎相同,当给药浓度增加,不可避免地对其它亚型产生抑制作用。所以寻求特异性抑制以降低副作用,对PI3K抑制剂的开发与治疗具有重要意义。
2018年SOLAR-1研究出炉,我们看到PI3Ka的选择性抑制剂alpelisib联合氟维司群可有效延长PIK3CA 突变患者的无进展生存,试验组可以达到11个月,获益5.3个月,且在原发性及继发性内分泌治疗耐药患者中均能看到改善。SOLAR-1的上佳表现直接促成了alpelisib这一口服小分子选择性PI3Kα抑制剂的新适应症的诞生。
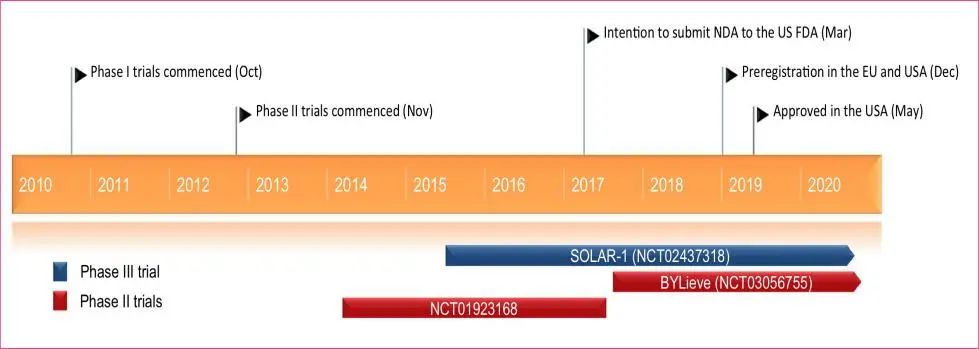
现阶段,CDK4/6抑制剂联合内分泌治疗已逐渐成为各大指南推荐治疗晚期HR+/HER2-乳腺癌的标准一线治疗方案,不可否认我们已经进入“CDK4/6i元年”。试问豪华阵容后出现耐药或复发转移,我们又该何去何从?在SOLAR-1中类似CDK4/6抑制剂治疗失败的患者占比非常少,2020年ASCO一项Ⅱ期临床研究:BYLieve试图进一步寻找这个问题的答案,队列A均是CDK4/6抑制剂+AI治疗失败的患者,给予Alpelisib+氟维司群治疗,主要观察终点为6个月无进展生存率,中位随访11.7个月。结果提示达到主要终点:6个月无疾病进展的患者比例为50.4%(95%CI:41.2%~59.6%),总缓解率ORR为17.4%,临床获益率可达45.5%。

和真实世界的选择化疗、更改内分泌药物等决策相比,Alpelisib+氟维司群交出了更漂亮的答卷:中位PFS达到了7.3个月。
PI3K家族功能太多,几乎介导所有细胞对胰岛素的反馈,牵一发而动全身。抑制PI3K相当于阻断了胰岛素作用通路,许多组织糖代谢会出现异常,导致血糖上升及后续毒性导致的停药与疗效的削弱。最应注意的是,高血糖引起的胰岛素反馈上调以及增加外源性胰岛素可进一步激活肿瘤细胞中的PI3K信号,削弱PI3Ki疗效。报道显示,这足以使小鼠肿瘤模型中PI3K信号重新激活,即使存在PI3K抑制剂,最终导致治疗耐药。
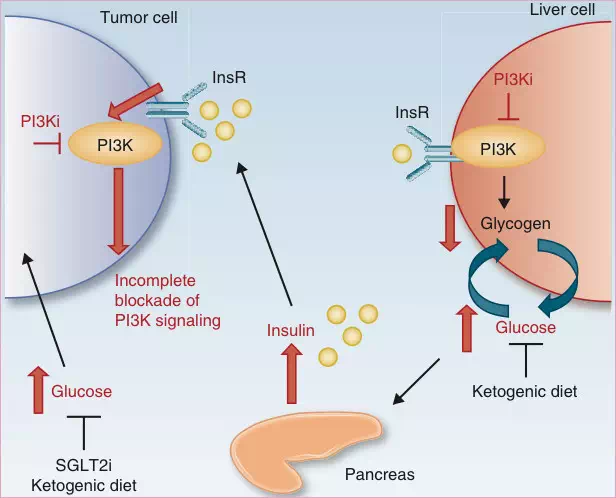
至于降糖处理的探索:
1、PI3K抑制剂抵消了二甲双胍激活AMP蛋白激酶的降糖机制,这是 “神药”二甲双胍介入临床探索却没能很好起到降糖作用的原因,也部分解释了SOLAR-1等研究治疗组更多胃肠道不良反应的现象;
2、生酮饮食能快速消耗肝糖原的储存,从而减少PI3K抑制剂带来的血糖上升,并增加机体对胰岛素的敏感性,减少体内的胰岛素水平。显著抑制血糖和胰岛素水平的上升,效果与另一类降糖药SGLT2抑制剂类似;
3、SANDPIPER研究中taselisib疗效在不同地区存在差别,亚洲风险比0.38,西欧/美国/加拿大/澳大利亚0.57,拉丁美洲/东欧1.18。患者胰岛素耐药程度、饮食和高血糖治疗的不同可以解释这种差异,这些结果表明生酮饮食的确有望弥补PI3K抑制剂的短板。
值得一提的是,与之前诸多PI3K抑制剂研究均止步于不可控的毒副反应不同,BYLieve研究表现出了较好的依从性与耐受性。最常见的≥3级不良反应包括高血糖(28%)、皮疹(9%)、腹泻(5.5%),此数据亦优于SOLAR-1研究。
Alpelisib还发现可以与BRAF抑制剂encorafenib和anti-EGFR单克隆抗体cetuximab共同用药可以降低毒性。
关于PI3K抑制剂的临床应用,未来还有如下几方面的问题等待进一步探索:
除了一些高频突变(PIK3CA基因中E542K、E545K和H1047R)的功能较为明确之外,中国人群特有突变、低频突变、罕见突变的功能与对应的敏感治疗尚不清楚。
PI3K抑制剂可以恢复细胞的雌激素依赖性,对于激素受体阳性的晚期乳腺癌,什么内分泌治疗才是与PI3Ki“最合拍的CP”?
PI3K抑制剂能有效阻滞PI3K,但癌细胞可通过激活下游的AKT和mTOR,对其产生耐药。将来的出路必定是多靶点的多重抑制?叠加的毒性如何把控?
对于HER2扩增乳腺癌患者,PI3K抑制剂联合抗HER2靶向药物有协同增效,初步发现优于赫赛汀+经典化疗的结果让我们颇为惊喜与期待。
SAFIR02研究发现10%的晚期三阴性乳腺癌存在PIK3CA的突变且生存数据更差。XUS06T研究探索联合白蛋白紫杉醇用于HER2阴性的晚期解救提示存在获益。初期数据之后,TNBC人群能否期待更深入的探索?
现实问题:在PI3Ki暂时国内不可及的情况下,在没有直接证据的前提下,mTORi可否是替代方案?不同突变位点是否又有不同的答案?
如上所述,作为逆转耐药与提高生存的重要通路,针对PI3Ki开发的抗癌药物在多次挫败后终有收获,能兼顾疗效与安全性的alpelisib初战告捷,带来惊喜。观而思,小分子大能量的广阔领域里仍然有大量基础与临床的问题等待我们去探索实践与回答,思考不止,步履不停,则未来可期。
1. Nandini Dey, Pradip De, Brian Leyland-Jones. PI3K-AKT-mTOR inhibitors in breast cancers: From tumor cell signaling to clinical trials. Pharmacol Ther. 2017; 175:91-106.2. Benoit Bilanges, York Posor, Bart Vanhaesebroeck. PI3K isoforms in cell signalling and vesicle trafficking. Nat Rev Mol Cell Biol. 2019 Sep;20(9):515-5343. Zhang M, et al. PI3K inhibitors: review and new strategies. Chem Sci. 2020 May 19;11(23):5855-5865.4. Chen L, et al. Characterization of PIK3CA and PIK3R1 somatic mutations in Chinese breast cancer patientsNat Commun. 2018 Apr 10;9(1):1357.5. Baselga J et al. Buparlisib plus fulvestrant versus placebo plus fulvestrant in postmenopausal, hormone receptor-positive, HER2-negative, advanced breast cancer (BELLE-2): a randomised, double-blind, placebo-controlled, phase 3 trial Lancet Oncol. 2017 Jul;18(7):904-916.6. Rinnerthaler G, Gampenrieder SP, Greil R.ASCO 2018 highlights: metastatic breast cancer. Memo. 2018;11(4):276-279.7. André F, Ciruelos E, Rubovszky G, et al. Alpelisib for PIK3CA-Mutated, Hormone Receptor-Positive Advanced Breast Cancer. N Engl J Med. 2019 May 16;380 (20):1929-1940.8. 2020 ASCO abstract 1006: Alpelisib + Fulvestrant in Patients With PIK3CA-Mutated Hormone-Receptor Positive (HR+), Human Epidermal Growth Factor Receptor-2-Negative (HER2–) Advanced Breast Cancer (ABC) Previously Treated With Cyclin-Dependent Kinase 4/6 Inhibitor (CDKi) + Aromatase Inhibitor (AI): BYLieve Study Results.9. Hopkins BD, et al. Suppression of insulin feedback enhances the efficacy of PI3K inhibitors. Nature. 2018 Aug;560(7719):499-503.10. 2020 ESMO Poster 352TiP :EPIK-B2: A Phase 3 Study of Alpelisib as Maintenance Therapy With Trastuzumab and Pertuzumab in Patients With PIK3CA-Mutated Human Epidermal Growth Factor Receptor 2-Positive (HER2+) Advanced Breast Cancer.11. 2018 ASCO Abstract 1018: Trial XUS06T: Phase I/II study of alpelisib and nab-paclitaxel in patients with locally recurrent or metastatic HER2− breast cancer.
四川省人民医院乳腺科 副主任医师 硕士生导师
四川省女医师协会乳腺专委会副主任委员
四川省抗癌协会乳腺专委会青年委员会副主任委员
四川省医师协会乳腺专委会青年委员会副主任委员
中国整形美容协会乳房修复与再造专业委员会委员
四川省整形美容协会乳房整形协会委员
中国医药教育协会乳腺疾病专委会委员





 京公网安备 11010502033352号
京公网安备 11010502033352号